神经生物学和遗传学团队
一、研究方向
神经生物学和遗传学团队现有教授2人,副教授1人,讲师2人。本团队主要结合遗传学、基因编辑、高通量动物行为检测和筛选、神经环路示踪、生物信息学以及蛋白质组学等多学科手段,深入研究以下几个科学问题:1)神经系统疾病的分子致病机制;2)睡眠和昼夜节律行为的神经调控机制;3)鱼类性控育种及其遗传机制研究。
团队成员先后承担国家自然科学基金和湖北省自然科学基金等多个项目,团队已在Nature Communications, PNAS, Cell Discovery, Molecular Psychiatry, Development, Molecular and Cellular Proteomics, Disease Models & Mechanisms、Molecular Phylogenetics Evolution、Journal of Neuroscience等高水平杂志上发表论文20余篇,获得专利2项。
二、团队成员

金珊,教授,团队负责人,中国湖北省细胞生物学会理事,2004年获得中国科学院水生生物所理学博士学位。研究领域为神经退行性疾病发病分子遗传机制及其相关基因功能解析。
Email: jinshan(AT)hubu.edu.cn

刘志华,教授,2011年获得中国科学院遗传与发育生物学研究所发育生物学博士学位。研究领域为睡眠和昼夜节律等行为调控的神经生物学机制,包括1)鉴定和解析调控睡眠长短和睡眠质量的关键基因和分子通路;2)环境变化对睡眠和昼夜节律行为的影响。
Email: zhihua_liu(AT)hubu.edu.cn

管波,副教授,2008年获得中国科学院水生生物研究所鱼类遗传学博士学位。研究领域为
鱼类遗传学和保护生物学相关研究。
Email: guanbo(AT)hubu.edu.cn

毛传樨,讲师,2014年获得湖北大学生物化学与分子生物学博士学位。研究领域为细胞骨架的动态调控与神经退行性疾病。
Email: cxmao(AT)hubu.edu.cn

熊英,讲师,2012年获得中国科学院遗传与发育生物学研究所发育生物学博士学位。研究领域为开发和利用质谱和蛋白质组学新技术和方法,揭示神经系统疾病的分子致病机制,鉴定用于疾病诊断或治疗的潜在生物标志物和靶点。
Email: ying.xiong(AT)hubu.edu.cn
三、研究成果
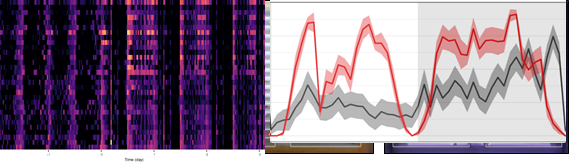
1. 高通量高精度果蝇睡眠监测和睡眠基因筛选平台:本实验室搭建了果蝇视频监测平台,能同时对 ~2000只果蝇的睡眠进行实时跟踪,实现高通量筛选睡眠调控的基因和神经环路。
 2. 学习记忆能力的成熟和衰老:本实验室发现关键神经元树突棘的生长和萎缩与与学习记忆能力的成熟和衰老相关,并发现调控这一过程的关键基因。
2. 学习记忆能力的成熟和衰老:本实验室发现关键神经元树突棘的生长和萎缩与与学习记忆能力的成熟和衰老相关,并发现调控这一过程的关键基因。
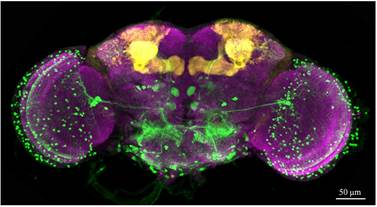
3. 神经发育障碍和微管的动态调控:本实验室通过新开发的微管可视化系统解析神经发育障碍相关基因在微管动态调控中的作用。
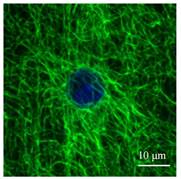
4. 鱼类性控育种及其遗传机制研究:通过鱼类雌核发育和激素性逆转等技术手段,控制黄颡鱼性别,实现YY超雄黄颡鱼规模化繁殖,实现全雄黄颡鱼产业化应用,获农业部批准水产新品种1个(黄颡鱼“全雄1号”登记号GS-04-001-2010)。

黄颡鱼“全雄1号”
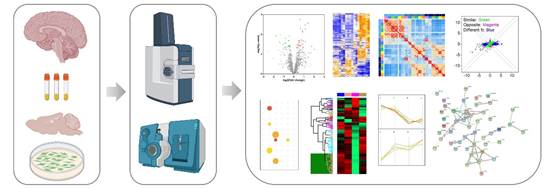
5. 基于先进质谱技术的蛋白质组学研究:利用细胞和动物模型以及病人样品,通过多组学数据整合分析和先进成像等方法,从分子和细胞水平揭示神经系统疾病的发病机制,筛选潜在药物靶点和生物标志物。
 四、承担科研项目(部分)
四、承担科研项目(部分)
1. 人类Kenny-Caffey综合症果蝇模型的建立及致病基因dTBCE功能解析,国家自然科学基金面上项目(2009.01-2011.12)
2. 微管剪切蛋白Katanin 60的功能解析,国家自然科学基金面上项目(2011.01-2013.12)
3. 微管乙酰化状态与tau微管毒性的关系,国家自然科学基金面上项目(2015.01-2018.12)
4. 磷转运蛋白对寿命调控的机理研究,国家自然科学基金面上项目(2019.01-2022.12)
5. 果蝇天蚕素B的果蝇细胞报答系统的建立及其产品应用研究,湖北省自然科学基金(2003.01–2005.12)
6. 长江中游水温节律变化对四大家鱼生殖周期的影响及其调控机制, 国家自然科学基金面上项目(2018.01–2021.12)
7. 三种单性黄颡鱼(XX\XY\YY)早期性腺分化相关基因差异表达研究,国家自然科学基金面上项目(2012.1–2015.12)
8. 圆口铜鱼卵母细胞体外成熟及雌核发育研究,湖北省自然科学基金(2009.12–2011.12)
五、 学术论文
5. Niu X, Mao CX, Wang S, Wang X, Zhang Y, Hu J, et al. (2023): alpha-Tubulin acetylation at lysine 40 regulates dendritic arborization and larval locomotion by promoting microtubule stability in Drosophila. PLoS One. 18: e0280573.
6. Xiong Y, Hong H, Liu C, Zhang YQ (2023): Social isolation and the brain: effects and mechanisms. Mol Psychiatry. 28:191-201.
7. Hong H, Zhao Z, Huang X, Guo C, Zhao H, Wang GD, et al. (2022): Comparative Proteome and Cis-Regulatory Element Analysis Reveals Specific Molecular Pathways Conserved in Dog and Human Brains. Mol Cell Proteomics. 21:100261.
8. Jia Y, Jin S, Hu K, Geng L, Han C, Kang R, Pang Y, Ling E, Tan EK, Pan Y, et al. Gut microbiome modulates Drosophila aggression through octopamine signaling. Nature Communications, 2021, 12(1), 2698.
9. Mao CX, Wen X, Jin S, Zhang YQ. Increased acetylation of microtubules rescues human tau-induced microtubule defects and neuromuscular junction abnormalities in Drosophila. Disease models & mechanisms, 2017, 1245-1252.
10. Ma X, Li X, Yi P, Wang C, Weng J, Zhang L, Zhu X, Jin S, Liu J. PiT2 regulates neuronal outgrowth through interaction with microtubule-associated protein 1B. Scientific Reports, 2017, 7:17850-17862.
11. Mao CX, Xiong Y, Xiong Z, Wang Q, Zhang YQ, Jin S. Microtubule-severing protein Katanin regulates neuromuscular junction development and dendritic elaboration in Drosophila. Development, 2014, 141:1064-1074.
12. Liu Z, Huang Y, Hu W, Huang S, Wang Q, Han J, Zhang YQ. Drosophila Acyl-CoA synthetase long-chain family member 4 inhibits synapse growth by attenuating bone morphogenetic protein signaling via endocytic recycling. Journal of Neuroscience, 2014, 34:2785-2796.
13. Xiong Y, Zhao K, Wu J, Xu Z, Jin S, Zhang YQ (2013): HDAC6 mutations rescue human tau-induced microtubule defects in Drosophila. Proc Natl Acad Sci U S A. 110:4604-4609.
14. Liu Z, Huang Y, Zhang Y, Chen D, Zhang Y. Drosophila acyl-CoA synthetase long-chain family member 4 regulates axonal transport of synaptic vesicles and is required for synaptic development and transmission. Journal of Neuroscience, 2011, 31(6):2052-2063.
15. Jin S, Pan L, Liu Z, Wang Q, Xu Z, Zhang YQ. Drosophila tubulin chaperone E functions at neuromuscular synapses and is required for microtubule network formation. Development, 2009, 136: 1571-1581.
16. Jin S, Hu GA, Qian YH, Zhang L, Zhang J, Qiu G, Zeng QT, Gui JF. Identification of one intron loss and phylogenetic evolution of Dfak gene in the Drosophilae melanogaster species group. Genetica, 2005, 125,223–230.
17. Guan B, Ma H, Wang Y, Hu Y, Lin Z, Zhu Z, Hu W*. Vitreoscilla hemoglobin (VHb) overexpression increases hypoxia tolerance in zebrafish (Danio rerio). Marine Biotechnology, 2011, 13, 336–344.(封面文章)
18. Liu H*, Guan B*, Xu J, Hou C, Tian H, Chen H. Genetic manipulation of sex ratio for the large-scale breeding of YY super-male and XY all-male yellow catfish (Pelteobagrus fulvidraco (Richardson)). Marine biotechnology, 2013, 15, 321–328.
19. Guan B, Hu W*, Zhang T, Wang Y, Zhu Z*. Metabolism traits of 'all-fish' growth hormone transgenic common carp (Cyprinus carpio L.). Aquaculture, 2008, 284, 217–223.
20. Guan B, Hu W*, Zhang T, Duan M, Li D, Wang Y, Zhu Z. Acute and chronic un-ionized ammonia toxicity to 'all-fish' growth hormone transgenic common carp (Cyprinus carpio L.). Chinese Science Bulletin, 2010, 55, 4032–4036.
六、 授权发明专利
1. HU, W., Zhu, Z., MA, H., Guan, B., HU, Y., Lin, Z. A recombinant gene which enhances the hypoxia tolerance in fish and the use thereof,USPTO(2013,授权专利号:8546644)
2. 刘汉勤,管波,田华,徐江,侯昌春,建立全雌黄颡鱼繁育种群的方法(2013,授权专利号:ZL 201310034096.9)




