近日,湖北大学生命科学学院、省部共建生物催化与酶工程国家重点实验室、药物高通量筛选技术国家地方联合工程研究中心魏子贡教授团队在基于结构的创新药设计领域方面取得新进展。
伪狂犬病毒是严重危害生猪养殖业的重要病原体,同时具有极高的人畜共患风险,研发有效治疗手段迫在眉睫。在前期工作中,该团队基于循环神经网络以及强化学习,基于HSV-1 DNA聚合酶抑制剂PNU-183792的结构启示,发现了先导化合物c14,抗PRV活性达到14 pM(Wei L., er al., ACS Omega.2025, 10, 3389-3397)。最近,该团队进一步发现经典抗菌药环丙沙星(Ciprofloxacin)具有潜在抗PRV活性,由此开启喹诺酮类化合物的系统性优化研究。
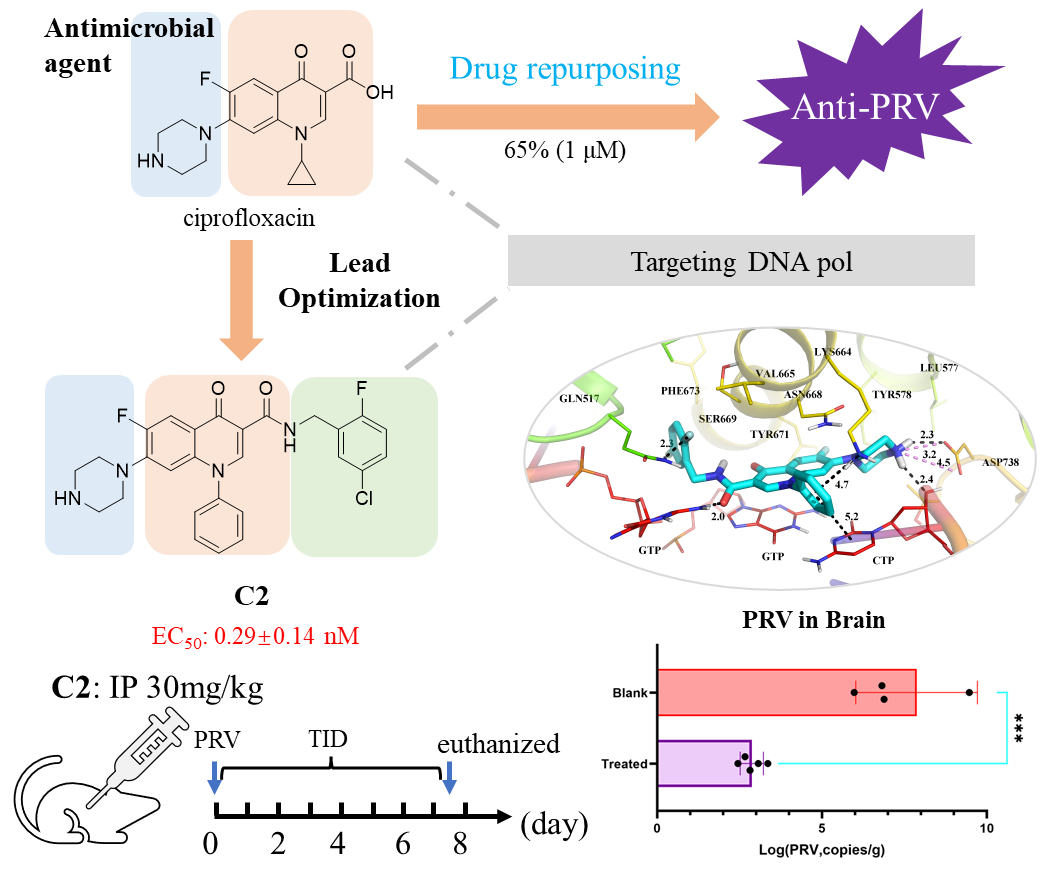
团队通过骨架跃迁技术,成功开发出优化化合物C2,实验数据显示,其EC50值低至0.29 nM,80%最小抑制浓度(MIC80)范围为1.6-8 nM,抗病毒活性较环丙沙星提升了超3000倍,展现出卓越的体外抗病毒效力。
在临床前研究中,C2表现出优异的药代动力学特性,经腹腔给药后血浆暴露量良好。小鼠感染模型显示,C2可显著抑制体内PRV复制,病毒载量降低达99%,且未观察到明显毒性反应。这一突破性进展证实了喹诺酮类化合物作为广谱抗疱疹病毒药物的开发潜力,为防控这一重要人畜共患病提供了全新解决方案。
C2的发现标志着基于结构设计的抗PRV药物开发迈出关键一步。其超强效力和良好成药性为后续临床转化奠定基础。目前,科研人员正推进C2的作用机制解析和安全性评价,以期尽快进入临床试验阶段。该成果不仅为动物疫病防控提供新武器,更为应对人畜共患病毒威胁开辟创新路径。相关成果有望推动喹诺酮类药物在抗病毒领域的老药新用,为应对新发突发传染病提供重要技术储备。
研究成果以《Rapid discovery of pseudorabies virus inhibitors repurposed from the antimicrobial agent ciprofloxacin》发表在《European Journal of Medicinal Chemistry》(中科院药物化学1区,湖北大学一类高水平杂志)(文章链接:https://www.sciencedirect.com/science/article/pii/S0223523425002557)。
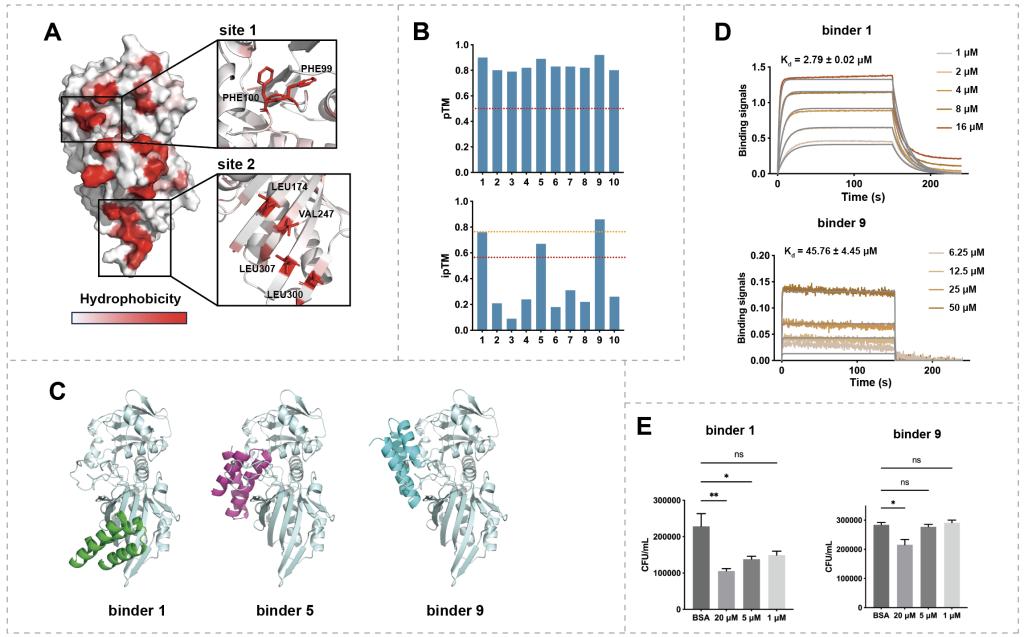
Mini-binder是介于抗体和小分子药物之间的一种全新大分子药物类型,因其兼具抗体和小分子的优点而成为近年来新药研发的热点。近日,团队在《International journal of biological macromolecules》(IF=7.7)发表题为“De novo designed mini-binders targeting glyceraldehyde-3-phosphate dehydrogenase of Streptococcus equi ssp. zooepidemicus provided partial protection in mice model of infection”的研究论文,报道了利用RFdiffusion蛋白质设计平台,针对SEZ黏附因子GAPDH的两个不同疏水位点设计mini-binder。经过pTM、ipTM等指标的严格筛选,最终确定并合成了3个mini-binder进行实验验证。团队从候选的设计中筛选发现binder 1与GAPDH具有微摩尔级亲和力,能显著抑制SEZ对HEp-2细胞的黏附。
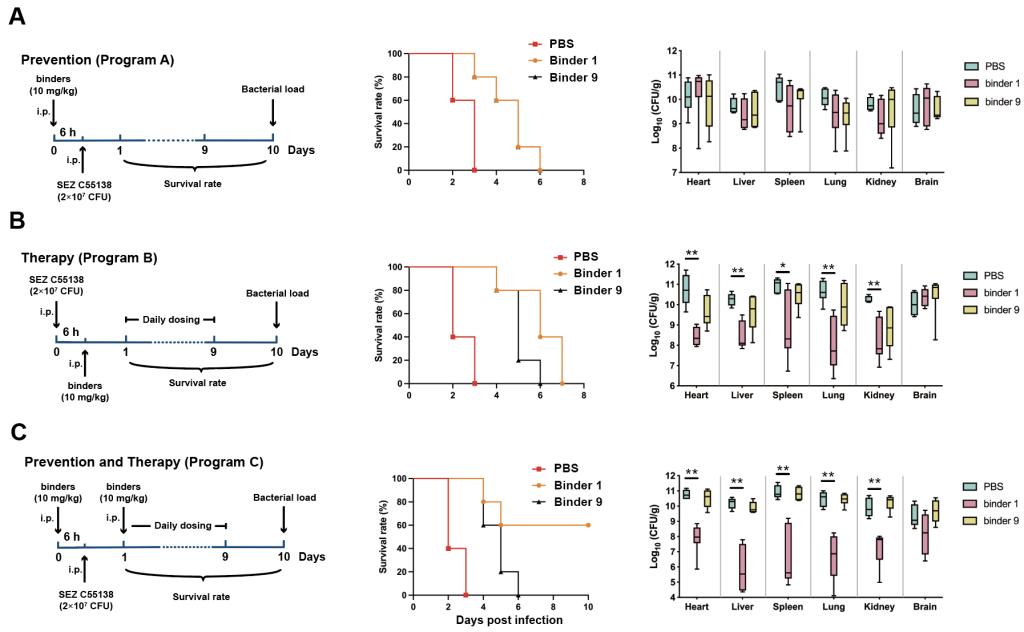
在动物模型中,Binder 1在不同的给药方式中均对致死剂量SEZ感染小鼠提供了保护作用,降低器官细菌载量;动物存活率最高可从0提高至60%,展现出显著的抗菌作用。
该研究是前期研究的延伸与扩展,为SEZ感染的防治提供新的解决方案,也为人工智能在大分子药物设计领域的应用开辟了新的方向(文章链接:https://doi.org/10.1016/j.ijbiomac.2025.142293)。
团队长期招收具有药学、计算机、生化与分子生物学、微生物学等学科背景的研究生,欢迎各位同学报考。
(审核人:李爱涛)
![]() 地址导航:湖北省武汉市武昌区友谊大道368号
地址导航:湖北省武汉市武昌区友谊大道368号![]() 邮政编码:430062
邮政编码:430062![]() 联系电话:(027)88664102
联系电话:(027)88664102
